 |  | |
Les réactions enzymatiques | ||
 |  |
Dans une réaction chimique simple, deux corps vont se recontrer et se combiner pour en former un troisième totalement nouveau. Selon l'énergie chimique stockée dans les composants de départ et d'arrivée ont pourra avoir trois cas :
Bien que la cellule utilise les trois types de réactions, le dernier est le plus courant.
Dans la plupart des cas, deux problèmes se posent. :
Le premier : à partir des composés de départ, on peut obtenir plusieurs produits. Tous seront produit, leur abondance relative dépendant de plusieurs paramètres. Mais en général, un seul de ses produits est désirée. L'homme peut en variant les conditions de réaction, favoriser un produit plutot qu'un autre, mais aucune solution efficace à 100% n'est disponible aujourd'hui, il y a toujours un déchet résultant des conditions expérimentales. La cellule en revanche est capable de sélectionner les produits fabriqués avec un taux de déchets nul.
Le second problème concerne la vitesse de réaction. En réalité une réaction chimique se produit en deux étapes :
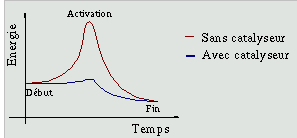 L'activation des réactifs nécessite de fournir de l'énergie.
Il y a donc une barrière de potentiel à passer pour que la
réaction se produise. C'est grace a cette barrière que les
réactions chimiques possibles ne se produisent pas intantanément
à tout instant, que par exemple l'essence ne s'enflamme pas instantanément
au contact de l'oxygène de l'air alors que cette réaction
est très exergonique. L'énergie nécessaire pour passer
cette barrière peut être fournie par l'energie cinétique
des réactifs et comme pour des molécules, énergie cinétique=chaleur.
Cela qui signifie qu'en chauffant on augmente le nombre de molécules
capables de passer la barrière. Toutefois, cela ne marche
pas dans le cas des molécules thermosensibles, comme c'est le cas
de la plupart des molécules de la vie.
L'activation des réactifs nécessite de fournir de l'énergie.
Il y a donc une barrière de potentiel à passer pour que la
réaction se produise. C'est grace a cette barrière que les
réactions chimiques possibles ne se produisent pas intantanément
à tout instant, que par exemple l'essence ne s'enflamme pas instantanément
au contact de l'oxygène de l'air alors que cette réaction
est très exergonique. L'énergie nécessaire pour passer
cette barrière peut être fournie par l'energie cinétique
des réactifs et comme pour des molécules, énergie cinétique=chaleur.
Cela qui signifie qu'en chauffant on augmente le nombre de molécules
capables de passer la barrière. Toutefois, cela ne marche
pas dans le cas des molécules thermosensibles, comme c'est le cas
de la plupart des molécules de la vie.
Il existe des composés qui ajouté aux réactifs
accélerent la réaction chimique mais se retrouvent intact
à la fin. Ces composés qui n''interviennent pas dans le bilan
global mais qui agissent par leur seule présence sont appelés
des catalyseurs. Ils ont la propriété de faciliter l'activation
des réactifs en abaissant la barrière de potentiel. Ces composés
ne fournissant, ni ne requérant pas d'énergie, ils n'interviennent
pas dans les proportions des équilibres, bien que il spuissent favoriser
certaines réactions aux dépend d'autres. Les catalyseurs
les plus performants utilisés aujourd'hui dans l'industrie sont
des poudres métalliques.
La cellule a résolu les deux problèmes à la fois au moyen d'une famille de molécules originale les enzymes.
Les enzymes sont les catalyseurs cellulaires. Ils sont constitués d'une charpente protéique associé à un groupement non protéique appelée groupement prosthétique. La protéine a deux fonctions :
La phase catalytique est assurée par le groupement prosthétique. Il s'agit d'une molécule organique non protéique, maintenue en place dans la structure au moyen de liaisons ioniques et hydrogènes. Au centre on trouve en général un atome métallique, comme quoi la nature utilise en fin de compte les mêmes solutions que l'homme, elles sont juste mieux exploitées. Les groupements prosthétiques appartiennent à plusieurs catégories moléculaires, le plus connu est l'hème intervient dans la plupart des réactions ou l'oxygène intervient (hémoglobine, hémocyanine) ou plus généralement dans les réactions d'oxydo-reduction (cytochrome, chlorophylle). Mais il en existe bien d'autre beaucoup appartenant à la famille des vitamines.
Les enzymes sont donc des catalyseurs hautement spécifiques. Ils obéissent toutefois aux mêmes lois que les catalyseurs classiques : ils ne modifient pas les proportions d'un équilibre dans une réaction reversible et ils ne peuvent pas fournir l'enrgie aux réactions qui en ont besoin. Les réactions exergoniques ne posent aucun problème, mais il existe des cas où ces deux conditions sont incompatibles avec les besoins de la cellule. Quand elle a en effet besoin de transformer une molécule en une autre elle ne peut pas se permettre de perdre une proportion non négligeable des réactifs, et certaines réactions nécessitent de fournir de l'énergie. La cellule a contouné ces deux moyens.
Le problèmes des quilibres est le suivant : un mélange de composé A va donner par catalyse enzymatique un mélange B. Simultanément les produits de B vont réagir pour redonner A. Sauf si l'un des composant de B n'est plus disponible. La réaction de retour ne peut plus se produite, seule la réaction désirée se produit et les composants de A vont totalement être transformés en B. C'est ainsi que la cellule procéde pour déplacer ses équilibres. La façon dont elle fait disparaitre l'un des produits varie. La méthode la plus courant est d'en faire le réactif d'une nouvelle réaction, ce qui va consommer le produit au fur et à mesure de sa production. C'est ainsi que les chaines métaboliques fonctionnent : une série de réactions se produisent chacune consommant les produits de l'étape précédente de la chaine, il suffit alors d'une seule réaction exergonique, donc irréversible, pour que toute les réactions de la chaine aille dans le même sens.
Le déplacement des équilibres n'est pas le seul moyen de la cellule pour résoudre ce problème. Elle peut aussi utiliser la méthode qui va suivre, qui permet normalement aux réaction endergoniques de se produire.
Les réactions endergoniques ont besoin d'énergie pour se dérouler. L'enzyme ne peut pas la fournir. En revanche elle est tout a fait capable de coupler deux réactions une endergonique et une exergonique. Le bilan global étant très exergonique, la réaction endergonique se déroulera tirée par la réaction exergonique. C'est ainsi que la molécule peut oxyder une molécule déja oxydée, ou augmenter l'acidité d'une molécule déjà acide. La cellule peut aussi coupler selon le même principe des réactions exergoniques à des phénomènes pûrement physiques gourmants en énergie comme par exemple la contraction musculaire.
Bien que les réactions exergoniques soient fort nombreuses au sein de la cellule, celle-ci n'en a selectionnés qu'un petit nombre. Cela lui permet d'assurer ses besoins en énergie à l'aide d'un petit nombre de molécules, dont l'implication dans les réactions précises (en général une hydrolyse) produit l'énergie. Ces molécules "batteries" sont riches en énergie. La plus courante est l'adénosine triphosphate (ATP), mais il en existe d'autres : tous les nucléotides triphosphatés, les dérivés du nicotinamide pour les réactions d'oxydoréduction. Mais après usage, ces molécules doivent être rechargé, certaines voies métaboliques assurent leur resynthèse à partir de leur produit de dégradation (AMP et ADP pour l'ATP) et d'une molécule chargée en énergie mais pas utilisable directement comme molécule batterie comme le glucose.
Une autre voie pour fournir l'énergie aux réactions endergoniques consiste encore en un couplage, mais ce coup ci avec un phénomène physique. Par exemple, le cytoplasme des bactéries est moins acides que la zone périmembranaire, il existe un gradient d'ion H+ entre l'intérieur et l'extérieur. Les ions H+ ont donc tendance à rentrer dans la cellule, produisant une force nommée proton motrice, la bactérie utilise cette force pour synthétiser l'ATP. Pour expulser les ions H+ et assurer la maintenance de la force proton motrice, d'autres réactions sont utilisées, comme la degradation du glucose par voie respiratoire ou la photosynthèse. Cette force proton motrice peut également être utilisée pour réguler la concentration intracellulaire de certains ions.
Les ribozymes, contraction de acide RIBOnucléique et enZYMES sont des enzymes particulières car elles ne sont pas constituées de protéines mais d'ARN. Elle sont encore peu connues car de découverte récente mais leur importance est grande. Ainsi on a constaté que plusieurs complexes protéiques impliqués dans la synthèse de l'ADN ou de protéines possédaient un coeur ribozymique qui assurait la réaction.
Toutefois, l'apport majeur de la découverte des ribozymes a été de fournir la réponse à un problème apparement insoluble : les protéines sont codées par l'ADN qui nécessite des protéines pour s'exprimer. Ce système est complexe et aucun des constituants ne peut exister sans l'autre (un peu comme le problème de la poule et de l'oeuf). La façon dont cela avait pu se mettre en place était inimaginable, aucun système plus simple tout en étant fonctionnel n'avait pu être trouvé. Le fait que l'ARN possède des propriétés catalytiques a apporté une solution : l'ARN peut exister sans les protéines. Il est moins efficace que les protéines car ses possibilités sont plus limitées, mais il est capable de réaliser les synthèses les plus importantes : protéines et acides nucléiques. Tout devenait clair si le modèle cellulaire actuel avait été précédé de cellules primitives basées sur un métabolisme à base d'ARN. De plus, l'existence d'ARN autoreproductile à permis de determiner que la séléction naturelle avait débuté très tôt dès la soupe primitive au niveau moléculaire. A partir de là, le développement de la vie était inévitable, seul le chemin qu'elle allait prendre restait à déterminer.